- Редактирование генома в стволовых клетках: будущее медицины или опасная игра?
- Что такое стволовые клетки и почему их так ценят?
- Технологии редактирования генома: как это работает?
- Редактирование генома в стволовых клетках: особенности и преимущества
- Практические применения редактирования генома в стволовых клетках
- Лечение наследственных заболеваний
- Регенерация поврежденных тканей
- Генетическая терапия рака
- Этические и правовые аспекты
- Будущее редактирования генома в стволовых клетках
Редактирование генома в стволовых клетках: будущее медицины или опасная игра?
Современная медицина стоит на пороге революционных перемен, и одной из самых обсуждаемых тем сегодня является редактирование генома. Особенно интересно применение этой технологии в области стволовых клеток. Именно благодаря способности стволовых клеток превращаться в любой тип ткани или органа, ученые рассматривают возможность коррекции генетических дефектов на самой ранней стадии развития человека. Этот подход обещает не только лечение наследственных заболеваний, но и возможность регенерации поврежденных тканей и даже органов.
На сегодняшний день технологии редактирования генома, такие как CRISPR-Cas9, преобразили подходы к терапии. Но как именно эти методы работают с такими особенными клетками, как стволовые? Какие перспективы и риски сопутствуют такой практике? В этой статье мы подробно расскажем о всех аспектах этой темы, поделимся мнением специалистов и расскажем, как развивается эта область на практике.
Что такое стволовые клетки и почему их так ценят?
Стволовые клетки — это уникальные клетки организма, которые обладают свойством самовосстановления и способны превращаться в разные типы тканей. Благодаря этим качествам, они считаются «строительным материалом» для организма. В медицинской лаборатории их применяют для регенерации поврежденных структур, лечения различных болезней и даже в генной терапии.
Существует несколько типов стволовых клеток:
- Эмбриональные стволовые клетки: получаются из эмбрионов и могут превращаться во все типы клеток организма.
- Преимплантационные клетки (пренефалные): находятся в ранних стадиях развития эмбриона.
- Местные или взрослые стволовые клетки: находятся в органах и тканях взрослых людей и помогают поддерживать и восстанавливать их функции.
Использование именно эмбриональных и преимплантационных стволовых клеток вызывает множество этических дискуссий, но именно они обладают наибольшим потенциалом для регенерации тканей при генной коррекции.
Технологии редактирования генома: как это работает?
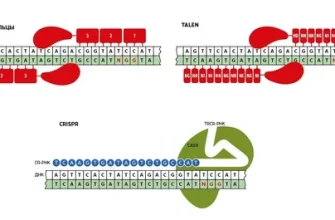
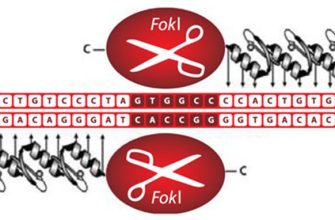
Главной технологией, используемой сегодня для редактирования генома, является CRISPR-Cas9. Эта система основана на природе бактериальных иммунных механизмов и представляет собой «инструмент», который позволяет точно вырезать или вставлять гены в определённые участки ДНК.
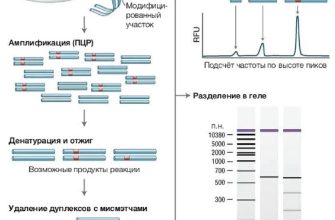
Основные этапы редактирования генома включают:
- Выбор цели: определение конкретного участка ДНК, который необходимо изменить.
- Создание гида: специальной молекулы, которая направляет систему CRISPR к нужной последовательности.
- Редактирование: «вырезание» некорректной части и вставка исправленного сегмента или отключение гена.
- Внедрение изменений: после этого происходят проверки, и новые гены интегрируются в клетки, создавая желаемую характеристику.
Именно это технологическое достижение открыло новые горизонты в медицине, позволяя не только исследовать гены, но и устранять их дефекты.
Редактирование генома в стволовых клетках: особенности и преимущества
Работа с стволовыми клетками — это особый вызов и одновременно большое преимущество. Благодаря их способности делиться и дифференцироваться, редактирование в этих клетках позволяет получить uniforme решения для определенного заболевания или патологии.
Основные преимущества включают:
- Многократное деление: после редактирования, клетки могут делиться и размножаться, распространяя исправленный геном по всему организму.
- Генетическая стабильность: при успешной коррекции гена, риск возникновения нежелательных мутаций снижается.
- Регенерация тканей: после интеграции редактированных клеток в организм, происходит восстановление поврежденных тканей или органов.
Практические применения редактирования генома в стволовых клетках
Лечение наследственных заболеваний
Одной из главных целей исследований является борьба с наследственными болезнями, такими как муковисцидоз, гемофилия, серповидноклеточная анемия. В терапевтических целях в лабораториях происходит редактирование генов у стволовых клеток пациентов, после чего клетки возвращаются в тело, восполняя дефекты.
Регенерация поврежденных тканей
В случае травм или заболеваний, например, повреждений позвоночника или сердечно-сосудистых заболеваний, внедрение редактированных стволовых клеток способствует естественной регенерации тканей и восстановлению функций органов.
Генетическая терапия рака
Борьба с онкологическими заболеваниями также включает использование редактированных стволовых клеток, которые могут «учиться» распознавать и уничтожать раковые клетки.
Этические и правовые аспекты
Несмотря на огромный потенциал, редактирование генома в стволовых клетках вызывает множество этических вопросов. Самое главное — возможность создания «дизайнерских детей» или появления генетически изменённых организмов. В большинстве стран существуют строгие законы, регулирующие такие эксперименты, и проведение подобных исследований требует согласия и прозрачности.
Дополнительно, существуют опасения по поводу возможных непредсказуемых последствий:
- Неконтролируемое распространение изменений — риск того, что исправленные гены могут передаваться потомству.
- Побочные эффекты: непредвиденные мутации или изменения в других участках ДНК.
- Этические дилеммы: использование эмбриональных стволовых клеток и вмешательство в генетическую структуру будущего человека.
Будущее редактирования генома в стволовых клетках
Область редактирования генома в стволовых клетках развивается очень динамично. Основные тренды включают совершенствование методов точности и безопасности, создание специальных «частных» технологий и расширение сферы применения. В ближайшие годы можно ожидать появления новых методов, которые уменьшат риск ошибок, и увеличат эффективность терапии.
Главные направления для будущего:
- Автоматизация и стандартизация процедур — для обеспечения массового применения в медицине.
- Разработка новых технологий редактирования, например, базовых редакторов, которые могут исправить генные мутации без повреждения ДНК.
- Этические рамки и законодательство — для гуманного и безопасного использования технологий.
- Клинические испытания и масштабные проекты — по лечению тяжелых заболеваний с помощью редактированных стволовых клеток.
Редактирование генома в стволовых клетках — это технология будущего, которая может полностью изменить подход к лечению болезней и восстановлению организма. Но вместе с тем, она требует осторожности, ответственности и четкого регулирования. В целом, потенциал огромен, и именно в ближайшие десятилетия мир увидит, насколько эти инновации станут безопасными и доступными для широкой публики.
Вопрос: Какие основные риски связаны с редактированием генома в стволовых клетках?
Ответ: Основные риски включают непредсказуемые мутации или побочные эффекты, возможность передачи изменений будущим поколениям, а также этические вопросы, связанные с вмешательством в генетическую структуру человека. Кроме того, существует риск возникновения неконтролируемых процессов размножения редактированных клеток, что может привести к нежелательным последствиям, например, развитию опухолей.
Подробнее
| редактирование генома у человека | CRISPR и генная терапия | стволовые клетки медицина | генно-коррекционные технологии | этические нормы генной инженерии |
| перспективы редактирования ДНК | генетическая терапия 2024 | регуляция генетических модификаций | секреты генной инженерии | дизайнерские дети риск |
| законодательство о генной терапии | технологии редактирования Генома | научные открытия в генной терапии | будущее медицинской генетики | этические дилеммы генной инженерии |
| генная терапия для эмбрионов | редактирование генома 2023 | риски и безопасность | гены и здоровье | генно-модифицированные организмы |