- Редактирование генома в клеточных культурах: революция в современной биотехнологии
- Что такое редактирование генома и зачем оно нужно?
- Основные методы редактирования генома в клеточных культурах
- CRISPR/Cas9
- TALENs
- ZFN, Zinc Finger Nucleases
- Применение редактирования генома в клеточных культурах
- Использование в медицине
- Исследование заболеваний
- Генетическая инженерия и биотехнологии
- Этические аспекты и вызовы
- Практическая часть: что нужно знать для работы с геномным редактированием в лаборатории?
- Перспективы развития и будущие тренды
Редактирование генома в клеточных культурах: революция в современной биотехнологии
В последние годы мир науки переживает настоящую революцию благодаря развитию технологий редактирования генома. Особенно это актуально для клеточных культур, лабораторных моделей, используемых для исследований болезней, разработки лекарств и генетической терапии. В нашей статье мы подробно расскажем, что такое редактирование генома, какие методы существуют, и каким образом эти технологии изменяют современную биотехнологию и медицину.
Что такое редактирование генома и зачем оно нужно?
Редактирование генома — это целенаправенное изменение последовательности ДНК в клетке, чтобы исправить, вставить или удалить определённые гены. Этот процесс позволяет учёным точечно влиять на генетическую информацию, делая возможным лечение наследственных заболеваний, создание устойчивых к болезням сельскохозяйственных культур и разработку новых методов терапии.
Клеточные культуры, такие как линии человеческих или животных клеток, активно используются в исследованиях, поскольку позволяют изучать последствия генетических изменений в контролируемых условиях. Механизм редактирования генома открывает широкие возможности для научных экспериментов и практических приложений — от создания моделей заболеваний до производства биопрепаратов.
Основные методы редактирования генома в клеточных культурах
На сегодняшний день существует несколько ключевых технологий, которые позволяют проводить точное редактирование ДНК. Ниже мы подробно разберём наиболее популярные из них.
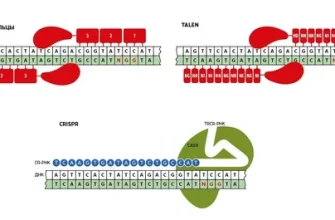
CRISPR/Cas9
CRISPR/Cas9, это революционная технология, которая позволяет легко и быстро редактировать гены в клеточных культурах. Этот метод основан на использовании системы иммунной защиты бактерий, адаптированной для наших целей. В основе — наличие специальной направляющей РНК, которая взаимодействует с целевым участком ДНК, и атома-фермента Cas9, который разрезает цепь ДНК в нужной точке.
- Механизм воздействия:
- Создаётся гена-специфическая РНК.
- РНК соединяется с ферментом Cas9.
- Комплекс ищет соответствующий участок ДНК в клетке.
- Индуцируется разрез, после чего происходит восстановление цепи, с возможностью вставки или удаления гена.
Преимущества: простота использования, высокая эффективность, возможность редактирования множества генов за раз.
TALENs
Талендомеры (Transcription Activator-Like Effector Nucleases, TALENs), это технологии, основанные на создании специальных нуклеаз, распознающих определённые последовательности ДНК. Они состоят из повторяющихся доменов, каждый из которых распознаёт конкретный нуклеотид.
- Эти нуклеазы можно программировать под любой участок ДНК, что делает их универсальными инструментами.
- После связывания они разрезают ДНК, вызывая процессы исправления и внедрения изменений.
Плюсы и минусы: высокая точность, но более сложная и дорогая по сравнению с CRISPR-технологией.
ZFN, Zinc Finger Nucleases
ZFN — это нуклеазы, состоящие из фингер-белков, распознающих последовательности ДНК, и фермента-обломщика. Эти белки специально проектируют под нужный участок гена. После связывания происходит разрез цепи ДНК, что стимулирует механизмы исправления, приводящие к желаемым изменениям.
Применение редактирования генома в клеточных культурах
Технологии редактирования генома находят широкое применение в различных сферах науки и медицины. Важно понять, какие возможности открывает эта технология и какие задачи она помогает решать.
Использование в медицине
Редактирование генома в клеточных культурах стало ключевым инструментом для разработки новых методов терапии наследственных заболеваний, таких как серповидноклеточная анемия или муковисцидоз. В лаборатории учёные создают генные модели этих болезней, что помогает лучше понять их механизм и искать эффективные лекарства.
Также редактирование используется для создания препаратов и вакцин, а в перспективе — для терапии онкологических и аутоиммунных заболеваний.
Исследование заболеваний
Многими исследовательскими группами создаются клеточные модели заболеваний с помощью целенаправленных изменений генов. Это позволяет изучать развитие болезней, проверять новые лекарства и оценивать потенциал генной терапии без риска для пациента.
Генетическая инженерия и биотехнологии
Создание устойчивых к вредителям и болезням сельскохозяйственных культур, биовакцин и биопрепаратов — все это результат применения технологий редактирования генома. В клеточных культурах разрабатываются и тестируются новые сорта и штаммы, что ускоряет процессы и снижает затраты.
Этические аспекты и вызовы
Несомненно, такие мощные технологии требуют ответственности. Важно соблюдать этические нормы, чтобы не допустить злоупотреблений, например, редактирование генома для создания «приспособленных» организмов или недопустимых вмешательств в человеческое потомство.
Кроме того, остаются вопросы безопасности, возможность случайных мутаций и последствия долгосрочного использования новых методов. Поэтому развитие подобных технологий требует строгого контроля и международного регулирования.
Практическая часть: что нужно знать для работы с геномным редактированием в лаборатории?
Работа с современными технологиями редактирования требует специальных знаний и навыков. Основные этапы включают:
- Подготовка образцов и выбор целевых генов.
- Разработка и синтез направляющих РНК или проектирование нуклеаз.
- Внедрение системы в клетки (метод электропорации, липосом, вирусных векторов).
- Обследование эффективности и точности редактирования (с помощью секвенирования).
- Анализ и подготовка данных для дальнейших исследований или терапии.
Для этого необходимо иметь представление о молекулярной биологии, генетике и технологии клеточного культивирования. Но главное — быть внимательно настроенными на получение качественных и безопасных результатов.
Перспективы развития и будущие тренды
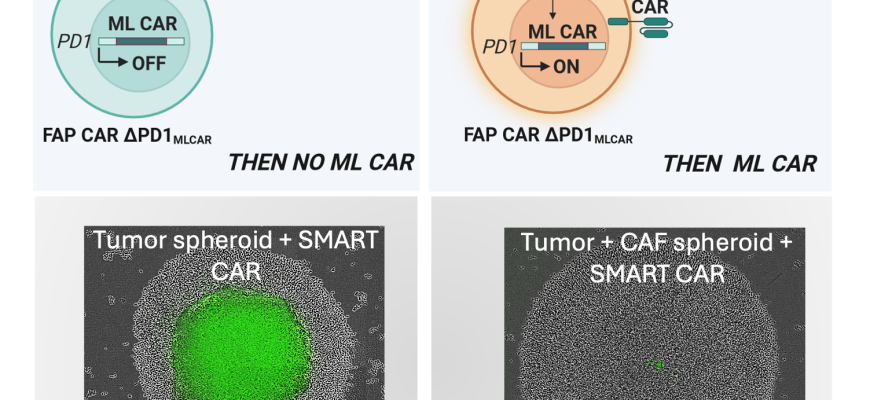
Технологии редактирования генома продолжают быстро развиваться. Ученые работают над повышением точности, снижением побочных эффектов и расширением спектра возможных целей. В перспективе появятся «умные» системы, способные автоматически вносить нужные изменения, а также — интеграция с искусственным интеллектом для анализа данных;
Наиболее ожидаемое — это возможность применять эти технологии для терапии у живых пациентов. Уже сейчас в лабораториях ведутся клинические испытания, которые могут в ближайшие годы стать новым стандартом лечения многих болезней.
Редактирование генома в клеточных культурах — это мощный инструмент, который меняет научный ландшафт, приближая нас к новым открытиям в медицине, сельском хозяйстве и биотехнологиях. Несмотря на наблюдаемые вызовы и этические проблемы, развитие данных технологий обещает светлое будущее, в котором границы между возможным и невозможным будут стираться. Важно помнить, что от ответственного использования зависит не только прогресс науки, но и благополучие всего человечества.
Вопрос: Почему редактирование генома считается революционной технологией, и чем она отличается от предшественников?
Ответ: Редактирование генома считается революционной технологией, потому что оно позволяет целенаправленно и эффективно изменять ДНК в конкретных участках, что ранее было очень сложным или невозможным с помощью методов, таких как случайное мутагенез или пересадка генов. В отличие от старых методов, современные технологии (например, CRISPR/Cas9) обеспечивают высокую точность, скорость и доступность редактирования, значительно ускоряя научные исследования и расширяя терапевтические возможности.
Подробнее
| генетическая инженерия в медицине | CRISPR-примеры в лаборатории | редактирование генома в клеточных культурах | методы генного редактирования | биотехнологические перспективы |
| редактирование гена у человека | преимущества CRISPR | законодательство и этика | новейшие исследования редактирования | применение в агробизнесе |