- Методы редактирования с использованием CRISPR-Base Editors: революция в генной инженерии
- Что такое CRISPR-Base Editors и как они отличаются от классического CRISPR-Cas9
- Виды CRISPR-Base Editors
- Механизм работы Base Editors
- Преимущества CRISPR-Base Editors
- Применение CRISPR-Base Editors в медицине и сельском хозяйстве
- Медицинские перспективы
- Сельское хозяйство и животноводство
- Таблица: Примеры использования CRISPR-Base Editors
- Этические и технические вызовы применения CRISPR-Base Editors
- Этические аспекты
- Технические сложности
- Краткая сводка основных технических вызовов:
- Будущее методов CRISPR-Base Editors: перспективы и разработки
Методы редактирования с использованием CRISPR-Base Editors: революция в генной инженерии
В мире современной биотехнологии одним из самых захватывающих и прорывных достижений последних лет стало появление методов редактирования генома с помощью CRISPR-Base Editors. Эти инновационные технологии открыли новые горизонты в медицине, сельском хозяйстве и фундаментальной науке. Вместе с нами вы познакомитесь с тем, как работают эти уникальные инструменты, какие преимущества они предоставляют и какие вызовы стоят перед учёными при их использовании.
Что такое CRISPR-Base Editors и как они отличаются от классического CRISPR-Cas9
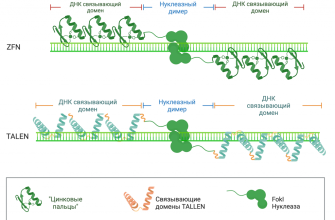
Классическая система CRISPR-Cas9 стала настоящим прорывом в области генной инженерии благодаря своей способности точно вырезать определённые участки ДНК. В её основе лежит использование направленных РНК молекул, которые привлекают Cas9 ─ белок, способный разрезать двойную спираль ДНК. Однако для изменения конкретных оснований потребуется создание новых методов, которые позволят изменить нуклеотиды без разрезания цепи. Именно здесь на сцену выходят CRISPR-Base Editors.
CRISPR-Base Editors – это специально разработанные ферменты, которые позволяют изменять отдельные нуклеотиды в ДНК без необходимости разрезания обеих цепей. Они основываются на мутациях классического Cas9, превращая его в «молекулу-редактор», которая способен выполнять точечные изменения всего за несколько часов.
Виды CRISPR-Base Editors
На сегодняшний день существует два основных типа CRISPR-Base Editors, каждый из которых предназначен для выполнения конкретных типов изменений нуклеотидов:
- Цитозиновые редакторы (CBEs) ─ преобразуют цитозин (C) в тимин (T), что фактически приводит к замене G•C на A•T в паре оснований.
- Урацилиновые редакторы (ABEs) ─ превращают урацил (U) в тимин (T), что соответствует замене A•T на G•C.
Механизм работы Base Editors
Основой работы CRISPR-Base Editors является использование ферментов, которые соединяются с гнездом, где должна произойти замена. В составе таких редакторов находятся:
- модифицированный Cas9 (dCas9 или нон-слепой Cas9) – не разрывает цепи, а удерживает фермент в нужной позиции;
- деацилирующие или деаминазные ферменты – выполняют химическую модификацию конкретных оснований;
- связующие связки и регуляторные элементы – обеспечивают целенаправленное действие и минимизацию побочных эффектов.
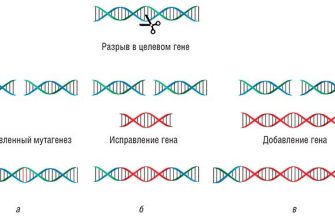
Когда гидаская РНК находит нужную последовательность ДНК, фермент активируется, и происходит преобразование необходимого нуклеотида, не разрывая основную цепь. В результате мы получаем точечную мутацию, которая может стать ключевым моментом в лечении генетических заболеваний или создании новых сортов растений.
Преимущества CRISPR-Base Editors
Это один из наиболее перспективных методов, поскольку он позволяет выполнять точечные изменения с высокой точностью и минимальной побочной активностью. Ниже представлены основные достоинства этих редакторов:
| Преимущество | Описание |
|---|---|
| Высокая точность | Изменения происходят только в заданных нуклеотидах, что снижает вероятность ошибок. |
| Меньше повреждений | Отсутствие разреза двойной цепи уменьшает риск нестабильных мутаций и повреждений генома. |
| Быстрота и эффективность | Изменения происходят за короткий промежуток времени и с высокой вероятностью успеха. |
| Применимость к различным видам | Могут применяться как в медицине, так и в инженерии растений и животных. |
Применение CRISPR-Base Editors в медицине и сельском хозяйстве
Многие специалисты сегодня видят в этих технологиях ключ к решению сложнейших задач современной науки. Рассмотрим основные примеры их использования в различных сферах жизни.
Медицинские перспективы
CRISPR-Base Editors открывают уникальные возможности для лечения наследственных заболеваний, таких как гемофилия, муковисцидоз, семейная гиперхолестеринемия. Точечные мутации, вызывающие эти болезни, можно исправлять без опасных побочных эффектов, присущих классическому CRISPR-Cas9. Уже ведутся клинические исследования и экспериментальные работы, которые показывают эффективность этой технологии.
Сельское хозяйство и животноводство
Использование Base Editors помогает создавать новые сорта растений, устойчивых к болезням и засухе, а также улучшать качество урожая. В животноводстве – повышать устойчивость к болезням, увеличивать производительность и адаптировать животных к экстремальным условиям.
Таблица: Примеры использования CRISPR-Base Editors
| Область применения | Пример | Преимущества |
|---|---|---|
| Генетическая терапия | Исправление мутантных генов при наследственных болезнях | Неинвазивность, высокая точность |
| Создание новых сортов растений | Устойчивость к засухе | Ускоренное получение урожая |
| Адаптация животных | Повышение устойчивости к болезням | Более эффективное производство |
Этические и технические вызовы применения CRISPR-Base Editors
Несмотря на впечатляющие достижения, использование новых методов редактирования генов вызывает немалое количество вопросов этического и технического характера. Перед учёными стоит задача обеспечить безопасность, достоверность и минимизировать риски непредвиденных последствий.
Этические аспекты
На сегодняшний день остро стоят вопросы о границах допустимого вмешательства в геном человека и других организмов. Важной проблемой является возможность создания «дизайнерских детей», а также риск появления поколений с недопустимыми изменениями. Не менее важной является прозрачность и контроль за исследованиями в этой области со стороны правительственных и международных организаций.
Технические сложности
Даже самые современные редакторы имеют ограничения. Иногда изменения происходят не так точно, как хотелось бы, или могут возникнуть побочные мутации. Также существуют сложности с доставкой редакторов внутрь клеток и геномных участков, что требует постоянного совершенствования технологий.
Краткая сводка основных технических вызовов:
- Недостаточная селективность и возможные побочные эффекты;
- Ограниченная возможность доставки ферментов в нужные клетки;
- Несовершенство методов оценки эффективности изменения;
- Проблемы с контролем за мутациями на уровне организма.
Будущее методов CRISPR-Base Editors: перспективы и разработки
Несмотря на существующие трудности, развитие CRISPR-Base Editors продолжает идти быстрыми темпами. Учёные постоянно работают над улучшением точности, расширением спектра возможных изменений и снижением рисков нежелательных эффектов. Уже сейчас ведутся исследования по созданию новых редакторов, которые смогут выполнять более сложные мутации, а также комбинировать возможности нескольких типов редакторов в одном ферменте.
Количество потенциальных применений, от терапии редких заболеваний до устойчивого сельского хозяйства, растёт с каждым месяцем. В будущем возможна интеграция этих технологий с другими инструментами генной инженерии, что откроет новые горизонты в здоровье, продовольственной безопасности и экологической устойчивости.
Вопрос: Насколько безопасно применять CRISPR-Base Editors в медицинских целях и как преодолеть возможные риски?
Ответ: Безопасность применения CRISPR-Base Editors в медицине зависит от строгого контроля за процедурой, разработки высокоточных алгоритмов и методов оценки риска. Сегодня ведутся масштабные исследования, разрабатываются стандарты и протоколы, позволяющие снизить вероятность побочных эффектов. Однако окончательное решение в вопросе безопасности появится только после проведения широкомасштабных клинических испытаний и долгосрочного мониторинга результатов.
Подробнее
| иммунитет | генетические болезни | редактирование ДНК | генные терапии | генетическая модификация |
| Иммунная система и CRISPR | Лечение генных заболеваний | Последствия редактирования DNA | Безопасность генной терапии | Этические аспекты генной модификации |